1. NOM DU MÉDICAMENT VÉTÉRINAIRE
ANTIDORM 5 MG/ML SOLUTION INJECTABLE POUR CHIENS ET CHATS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
|
Chaque mL contient : |
|
|
|
|
|
Substance active : |
|
|
Atipamézole ……………………………………………………… |
4,27 mg |
|
(sous forme de chlorhydrate) |
|
|
(soit 5 mg de chlorhydrate d’atipamézole) |
|
Excipients :

Solution limpide et incolore.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Chiens et chats.
3.2 Indications d'utilisation pour chaque espèce cible
Inversion des effets sédatifs de la médétomidine ou de la dexmédétomidine.
3.3 Contre-indications
Ne pas utiliser en cas d’hypersensibilité à la substance active ou à l’un des excipients.
Ne pas utiliser chez les animaux reproducteurs.
Ne pas utiliser chez les animaux présentant une insuffisance hépatique, rénale ou cardiaque.
Voir aussi rubrique 3.7.
3.4 Mises en garde particulières
Aucune.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
L'atipamézole n'inverse pas l'effet de la kétamine, ce qui peut causer des convulsions chez le chien et entraîner des crampes chez le chat lorsque l'effet de la kétamine persiste seul. Ne pas utiliser l'atipamézole dans les 30 à 40 minutes après l'administration de kétamine.
Après l'administration du médicament vétérinaire, les animaux doivent être laissés au repos dans un endroit calme. Au cours de la phase de récupération, les animaux ne doivent pas demeurer sans surveillance. S'assurer que l'animal a retrouvé un réflexe de déglutition normal avant de lui proposer un aliment ou une boisson.
Compte tenu des variations de doses, il est recommandé lors d'un usage hors AMM d'administrer avec précaution le produit chez les animaux autres que les espèces cibles.
Si d'autres sédatifs que la (dex)médétomidine sont administrés, il faudra tenir compte du fait que les effets de ces autres agents sont susceptibles de persister après l'inversion des effets de la (dex)médétomidine.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Du fait de sa puissante activité pharmacologique, tout contact de l'atipamézole avec la peau, les yeux et les muqueuses doit être évité. En cas d'éclaboussures accidentelles sur la peau, lavez immédiatement la zone concernée avec de l'eau courante et propre. Demandez un avis médical si les irritations persistent et montrez la notice ou l'étiquette au médecin. Retirez les vêtements contaminés qui sont directement en contact avec la peau.
Des précautions doivent être prises pour éviter toute ingestion ou auto-injection accidentelle. En cas d'auto-injection ou d'ingestion accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l'étiquette. Ne pas conduire. Le patient ne doit pas être laissé seul.
Précautions particulières concernant la protection de l'environnement
Sans objet.
Autres précautions
3.6 Effets indésirables
Chiens et chats :
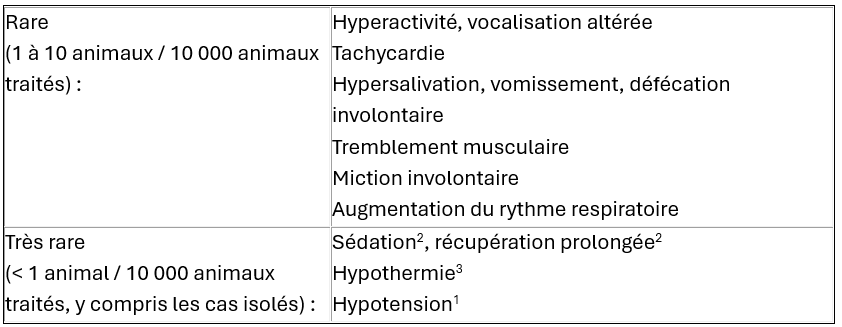
1 Transitoire, au cours des 10 premières minutes qui suivent l'injection.
2 Sédation récurrente pouvant survenir, ou le temps de récupération peut ne pas se trouver raccourci suite à l'administration d'atipamézole.
3 Chez les chats, en cas d'administration de faibles doses d'atipamézole pour inverser partiellement les effets de la médétomidine ou de la dexmédétomidine, toutes les précautions nécessaires devront être prises afin d'éviter l'hypothermie (même après le réveil de l'animal).
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
L'innocuité du médicament vétérinaire n'a pas été établie en cas de gestation et de lactation.
Gestation et lactation :
Utilisation non recommandée durant la gestation et la lactation.
3.8 Interactions médicamenteuses et autres formes d'interactions
L'administration simultanée d'atipamézole avec d'autres médicaments actifs sur le système nerveux central comme le diazépam, l'acépromazine ou les opiacés n'est pas recommandée.
3.9 Voies d'administration et posologie
Voie intramusculaire. Pour injection unique.
La dose dépend de la dose de médétomidine ou de dexmédétomidine administrée au préalable.
Chiens :
La dose d'atipamézole, exprimée en µg de substance active par kg de poids corporel est égale à 5 fois la dose de médétomidine ou 10 fois la dose de dexmédétomidine utilisées au préalable.
Compte tenu de la concentration en atipamézole du médicament vétérinaire qui est 5 fois supérieure à celle des solutions à 1 mg de médétomidine et 10 fois supérieure à celle des solutions à 0,5 mg de dexmédétomidine, il suffit d'injecter un volume équivalent de chacune des solutions.
Compte tenu de la concentration en atipamézole du produit qui est 50 fois supérieure à celle des solutions à 0,1 mg de dexmédétomidine, il sera nécessaire d'injecter un volume 5 fois plus faible de la solution d'atipamézole.
Exemple de dosage chez les chiens :
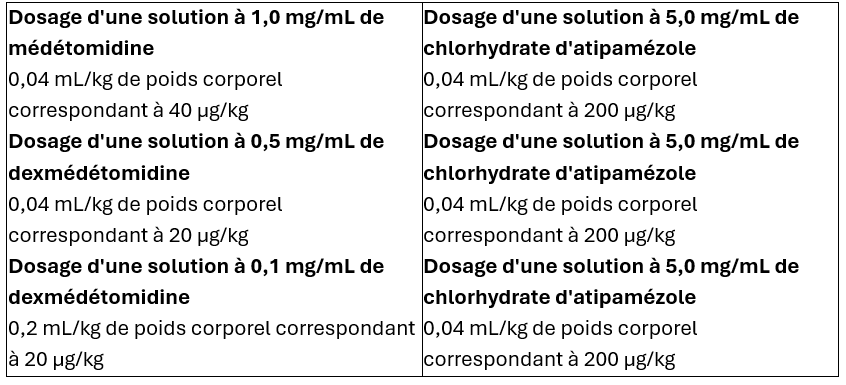
Chats :
La dose d'atipamézole, exprimée en µg de substance active par kg de poids corporel est égale à 2,5 fois la dose de médétomidine ou 5 fois la dose de dexmédétomidine utilisées au préalable.
Compte tenu du fait que la concentration en atipamézole du médicament vétérinaire est 5 fois supérieure à celle des solutions à 1 mg de médétomidine et 10 fois supérieure à celle des solutions à 0,5 mg de dexmédétomidine, il suffit d'injecter un volume équivalent de la moitié du volume des solutions de médétomidine ou de dexmédétomidine.
Compte tenu de la concentration en atipamézole du produit qui est 50 fois supérieure à celle des solutions à 0,1 mg de dexmédétomidine, il sera nécessaire d'injecter un volume 10 fois plus faible de la solution d'atipamézole.
Exemple de dosage chez les chats
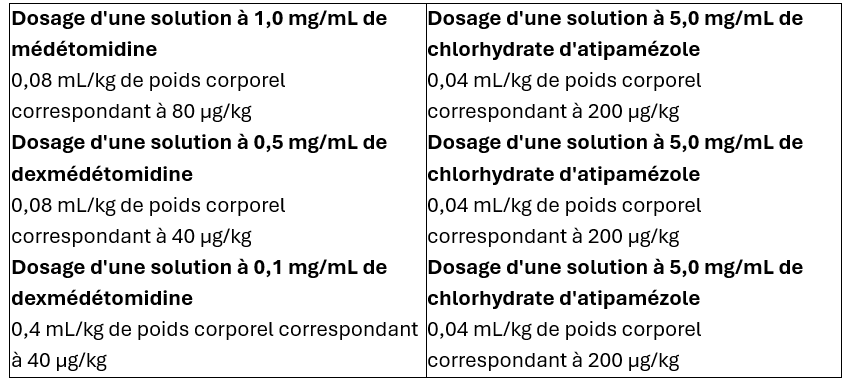
L’atipamézole est administré 15 à 60 minutes après l’injection de médétomidine ou de dexmédétomidine. Le temps de récupération des chiens et des chats est ramené à environ 5 minutes. Les animaux retrouvent leur mobilité environ 10 minutes après l'administration du produit.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
Un surdosage de chlorhydrate d'atipamézole peut entraîner une tachycardie transitoire ou une surexcitation (hyperactivité, tremblements musculaires). Si besoin, ces symptômes peuvent être inversés par l'administration d'une dose de chlorhydrate de médétomidine ou de dexmédétomidine inférieure à la dose clinique habituellement utilisée.
En cas d'administration par inadvertance de chlorhydrate d'atipamézole à un animal non traité au préalable avec du chlorhydrate de médétomidine ou de dexmédétomidine, des phénomènes d'hyperactivité, et de tremblements musculaires pourront se produire. Ces effets peuvent persister pendant environ 15 minutes.
Une surexcitation chez le chat peut être plus facilement gérée en minimisant les stimuli extérieurs.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Délivrance interdite au public.
Administration exclusivement réservée au vétérinaire.
3.12 Temps d'attente
Sans objet.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QV03AB90
4.2 Propriétés pharmacodynamiques
L'atipamézole est un agent sélectif et puissant qui bloque les récepteurs α2 (antagoniste α2) ce qui induit la libération d'un neurotransmetteur, la noradrénaline, dans le système nerveux central et périphérique. Il en résulte une activation du système nerveux central par activation sympathique. Les autres effets pharmacodynamiques pouvant être observés, par exemple sur le système cardiovasculaire, sont légers. En revanche, une baisse transitoire de la pression sanguine peut être observée dans les 10 premières minutes qui suivent l'injection de chlorhydrate d'atipamézole.
En tant qu'antagoniste α2, l'atipamézole est capable d'éliminer (ou d'inhiber) les effets d'agonistes des récepteurs α2 tels que la médétomidine ou la dexmédétomidine. Ainsi, l'atipamézole inverse les effets sédatifs du chlorhydrate de (dex)médétomidine chez les chats et les chiens, dont l'état revient à la normale et peut s'accompagner d'une augmentation transitoire du rythme cardiaque.
4.3 Propriétés pharmacocinétiques
Le chlorhydrate d'atipamézole est absorbé rapidement après injection intramusculaire. Il est également rapidement et complètement métabolisé. Les métabolites sont excrétés principalement dans l'urine et en petite quantité dans les fèces.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
En l'absence d'études de compatibilité, ce médicament vétérinaire ne doit pas être mélangé avec d'autres médicaments vétérinaires.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 30 mois.
Durée de conservation après première ouverture du conditionnement primaire : 28 jours.
5.3 Précautions particulières de conservation
Ce médicament vétérinaire ne nécessite pas de précaution particulière de conservation y compris après première ouverture du flacon.
5.4 Nature et composition du conditionnement primaire
Flacon en verre incolore type I contenant 10mL, muni d’un bouchon bromobutyle enrobé d'un polymère fluoré avec une capsule aluminium avec plastique flip-off.
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
VETPHARMA ANIMAL HEALTH S.L.
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/8813686 2/2013
Boîte en carton de 1 flacon de 10 mL
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
17/07/2013
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
29/01/2025
10. CLASSIFICATION DES MÉDICAMENTS VÉTÉRINAIRES
Médicament vétérinaire soumis à ordonnance.
Délivrance interdite au public.
Administration exclusivement réservée au vétérinaire.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).
IRCP 18/02/2025
